A pioglitazona é um medicamento da classe das tiazolidinedionas (TZDs) e atua por meio do receptor gama ativado por proliferadores de peroxissomos (PPAR-γ). O receptor PPAR-γ é expresso de forma mais abundante no tecido adiposo, mas também é encontrado em células beta pancreáticas, no endotélio vascular e em macrófagos. No fígado, no coração e no músculo esquelético, é expresso em menor proporção 1-3.
Indicações da pioglitazona:
A pioglitazona é indicada para o tratamento do Diabetes Mellitus do tipo 2 (DM2), como adjuvante às medidas ancilares de dieta e exercício. Pode ser usada em monoterapia ou associada a outros antidiabéticos orais, como metformina, sulfonilureias, semaglutida oral, inibidores do cotransportador sódio-glicose 2 (iSGLT2), agonistas dos receptores do GLP-1 injetáveis (Ex.: liraglutida, semaglutida, dulaglutida), agonista GLP-1/GIP (tirzepatida) e, em casos selecionados, coadjuvante ao tratamento com insulina 4,5.
Em consonância com as diretrizes brasileiras 4 e com o Standard of Care da American Diabetes Association 5 para o tratamento medicamentoso do DM2, Khan et al.6 conduziram uma revisão sistemática e uma meta-análise de estudos com pioglitazona em adição à metformina e à dapagliflozina. Três estudos randomizados e controlados (ERC) com 885 pacientes foram meta- analisados. A pioglitazona, adicionada à combinação metformina-dapagliflozina, mostrou-se segura, melhorando significativamente a glicemia de jejum, HbA1c e reduzindo o HOMA-IR. Além disso, aumentou a chance de atingir HbA1c < 7% (RR: 2,09; IC 95%: 1,66 a 2,64; p < 0,00001;
I2= 0%) e HbA1c < 6,5% (RR: 2,19; IC 95%: 1,36 a 3,53; p= 0,001; I2= 0%).6
Embora não esteja contemplada na bula, a pioglitazona pode ser usada no tratamento do pré- diabetes, como opção “fora de bula”, com o objetivo de prevenir a evolução para DM2, como demonstrado no estudo ACT NOW 7. Nesse estudo, houve uma redução de 72% nos novos casos de DM2, e a normoglicemia foi alcançada em 48% dos pacientes no grupo da pioglitazona, em comparação com 28% no grupo placebo 7.
Da mesma forma, pode ser utilizada no tratamento da esteatohepatite associada à disfunção metabólica, (metabolic dysfunction–associated steatohepatitis - MASH), sendo recomendada por diversas diretrizes recentes, nacionais e internacionais 8-10. A recente diretriz brasileira sobre a doença hepática esteatótica associada à disfunção metabólica (metabolic dysfunction- associated steatotic liver disease - MASLD), publicada conjuntamente pela Sociedade Brasileira de Endocrinologia e Metabologia (SBEM), Sociedade Brasileira de Hepatologia (SBH) e Associação Brasileira para Estudo da Obesidade e Síndrome Metabólica (ABESO), recomenda o uso da pioglitazona em pacientes com sobrepeso ou obesidade e MASLD, com esteatohepatite confirmada, independentemente da presença de fibrose (Recomendação 39; grau de recomendação e evidencia I,A) 9. Estas recomendações se baseiam em estudos clínicos randomizados e meta-análises que confirmam os efeitos benéficos da pioglitazona na melhora da esteatose, da inflamação e da fibrose hepáticas.
Posologia: A posologia recomendada é de 15 a 30 mg uma vez ao dia. Alguns estudos com dose menor (7,5 mg) também se mostraram eficazes. Entretanto, não dispomos dessa apresentação no mercado brasileiro.
Mecanismo de Ação:
O PPAR-γ é considerado o regulador “master” da adipogênese 1,2. A ativação desse receptor aumenta a proliferação de novos adipócitos e condiciona maior captação e estocagem de ácidos graxos livres (AGL), reduz seus níveis circulantes, melhora a sensibilidade à insulina (SI) e a função das células beta (Cel-β) pancreáticas, ao controlar o efeito lipotóxico sobre estas células. Exerce uma ação direta na resistência insulinica (RI) ao sequestrar os AGL (hipótese do “fatty acid steal”) e uma ação indireta por meio das adipocinas, como aumentar a adiponectina e reduzir as adipocinas inflamatórias (TNF-α, resistina, angiotensinogênio, PAI-1 e outras). Concomitantemente, melhora a sensibilidade à insulina no tecido adiposo e reduz a lipólise.
Entre as TZDs, a pioglitazona é única por atuar também como agonista fraco do PPAR-α11, caracterizando-a como um agonista duplo. O PPAR-α é mais difusamente expresso e mais abundante em tecidos com grande capacidade de metabolizar ácidos graxos, como fígado, intestino, tecido adiposo marrom, coração, rim e músculo esquelético 1,2,11. A ação sobre o PPAR- α explica seu efeito favorável na redução dos triglicerídeos e dos VLDL e no aumento do HDL- C, num efeito similar ao dos fibratos.
Farmacocinética e Farmacodinâmica do cloridrato de pioglitazona: 12
Absorção: Rápida após administração oral, com concentrações plasmáticas máximas entre 2 e 4 horas. A presença de alimentos pode atrasar levemente o pico, mas não altera a extensão total da absorção.
Distribuição: apresenta alta taxa de ligação às proteínas plasmáticas (>99%), principalmente à albumina. O volume de distribuição aparente é de aproximadamente 0,63 L/kg.
Metabolismo: Extensivamente metabolizado no fígado, por meio de reações de oxidação e hidroxilação, principalmente pelas enzimas CYP2C8 e CYP3A4. Gera metabólitos ativos importantes, como o M-III e M-IV.
Excreção: Eliminado predominantemente pelas fezes e pela bile após a metabolização. A meia- vida sérica da pioglitazona varia entre 3 e 7 horas. Portanto, deve ser administrada uma vez ao dia.
Efeitos pleiotróficos da pioglitazona:
A pioglitazona é um potente sensibilizador da insulina nos músculos, no fígado e no tecido adiposo. A melhora da sensibilidade à insulina no DM2 ocorre por meio de múltiplos mecanismos:
ativação de PPAR-γ, aprimoramento da sinalização da insulina, aumento do transporte de glicose, aumento da síntese de glicogênio, melhoria da função mitocondrial e mobilização de gordura para fora do músculo e do fígado. Como já discutido acima, ao melhorar a SI no tecido adiposo, reduzem-se a lipólise e a lipotoxicidade (revisto por Eldor et al.) 2. Estudos sugerem que os efeitos metabólicos das TZDs são mediados pelos seus alvos mitocondriais, mTORC1 e mTORC2, que atuam como transportadores de piruvato. Além disso, aumentam a expressão do coativador-1 do PPAR-γ (PGC-1), o regulador mestre da biogênese mitocondrial. O aumento do PGC-1 regula positivamente múltiplos genes da fosforilação oxidativa mitocondrial, aumentando a oxidação de gordura e diminuindo os níveis de metabólitos lipídicos intracelulares tóxicos.
Um dos efeitos mais importantes das TZDs é a preservação ou a melhora da função da Cel-β2, 13,14. Num estudo seminal, Gastaldelli et al.14 demonstraram que o índice de disposição da Cel-β foi significativamente melhorado com pioglitazona em pacientes diabéticos naives (+1,8 ± 0,7) e um pouco menos em pacientes sob tratamento com sulfonilureia (+0,7 ± 0,3), em comparação com o placebo (0,2 ± 0,3; P < 0,01). Interessantemente, a melhora na secreção de insulina correlacionou-se positivamente com o aumento do peso corporal (vide discussão adiante), da massa de gordura e da taxa de desaparecimento da glicose (Rd) e inversamente com a diminuição da glicemia plasmática e dos AGL durante um teste oral de tolerância à glicose (TOTG). Os resultados foram semelhantes em um terceiro grupo tratado com rosiglitazona, sugerindo que, nesse aspecto, as TZDs têm efeito semelhante.14
Prevalência e Importância do Diagnóstico de Pré-DM, DM2 e MASLD
O diagnóstico de pré-diabetes, DM2 e MASLD ganha importância diante da alta prevalência de obesidade no mundo, assim como da maior expectativa de vida da população. Estima-se que 33% da população brasileira com mais de 50 anos tenha diagnóstico de pré-diabetes15, o que representa um risco 20 vezes maior de evolução para DM2. Considerando o impacto de fatores socioeconômicos na prevalência de DM2, dos Santos, ESM et al.16 compararam dados do Brasil e da Inglaterra, mostrando maior prevalência de DM2 no Brasil (20%), enquanto a prevalência foi de 9,6% na Inglaterra. Essa maior prevalência no Brasil foi atribuída às diferenças na alimentação, bem como à dificuldade de acesso a instituições de saúde.16
Além do risco aumentado de DM2 em pessoas com pré-diabetes, a hiperglicemia é um fator de risco contínuo para complicações microvasculares e macrovasculares; ou seja, quanto maior o tempo de exposição e pior o controle glicêmico, maior o risco de complicações. Assim, pacientes com pré-diabetes podem apresentar complicações relacionadas à hiperglicemia. Estima-se que, no momento do diagnóstico do DM2, 8% a 16% dos pacientes já apresentem retinopatia, 17% a 22% já tenham microalbuminúria e 14% a 48% já tenham algum grau de neuropatia periférica. 15 De outra forma, o pré-diabetes está associado a maior incidência de doença cardiovascular e de mortalidade total, tanto na população geral quanto naqueles com doença aterosclerótica prévia.17
Em 2024, um total de 589 milhões de pessoas entre 20 e 79 anos, em todo o mundo, conviviam com diabetes. Entre os 10 países com maior prevalência, o Brasil ocupava o sexto lugar, com
16,6 milhões de pessoas (Diabetes Atlas)18. A prevalência de diabetes entre adultos nos Estados Unidos entre agosto de 2021 e agosto de 2023, segundo dados recentes do National Health and Nutrition Examination Survey19 era de 15,8%, dos quais 11,3% diagnosticados e 4,5% não diagnosticados. É importante entender que, se cerca de 16 pessoas tinham sido diagnosticadas, 5 não tinham sido. Portanto, supõe-se que não estavam em tratamento. Era maior em homens, aumentava com a idade e o peso, e era menor com maior nível de formação educacional.19
Por outro lado, pacientes com pré-diabetes, em geral, são portadores de RI e de síndrome metabólica (SMetab), o que lhes confere maior risco de doença cardiovascular aterosclerótica (DCVA) 20-23. De fato, inúmeros estudos e meta-análises, confirmam que a RI, per se, é um fator independente de RCV. 20,21 Um método simples de avaliar a RI em indivíduos não portadores de DM2 é o HOMA-IR: com efeito, o risco relativo de desfechos cardiovasculares aumenta substancialmente a cada aumento de 1 desvio padrão do HOMA-IR.20 A Smetab é um importante e, provavelmente, o mais frequente fator de risco cardiovascular e de DM2 da atualidade.22,23 No Brasil, por exemplo, uma revisão sistemática e meta-análise de estudos publicados entre 2011 e 2021, (26 estudos, 84.522 participantes) revelou uma prevalência da SMetab de 33% na população adulta, sendo 26% em homens e 38% em mulheres.24 Por óbvio, embora seja pauta de debates,25 a situação de pré-diabetes deve ser alvo de tratamento medicamentoso ou não, a fim de mitigar os riscos elevados associados a esta condição. É importante, portanto, utilizar métodos diagnósticos de alcance populacional e com boa sensibilidade. Por isso, a Federação Internacional de Diabetes propôs novos critérios e metodologia para o teste oral de tolerância à glicose (TOTG) de apenas 1 hora, valorizando e estabelecendo novo ponto de corte para a glicemia aos 60 minutos, conforme tabela abaixo 26:
Tabela 1: GLICEMIA DE 1 HORA APÓS SOBRECARGA DE GLICOSE Ref 26
|
Normal |
Pre-diabetes |
Diabetes |
|
≤154 mg/dL |
155–208 mg/dL |
≥209 mg/dL |
A MASLD, anteriormente denominada doença hepática gordurosa não alcoólica (NAFLD), é atualmente a doença hepática crônica mais prevalente no mundo. Está associada a um maior risco de cirrose e de carcinoma hepatocelular (CHC), com impacto crescente na morbimortalidade hepática, cardiovascular e metabólica.27-29 Estima-se que sua prevalência atinja cerca de um terço da população global, acompanhando o aumento da obesidade, do DM2 e da Smetab.30 No Brasil, estudos demonstram um cenário igualmente preocupante, com progressão significativa para fibrose avançada, cirrose e CHC, frequentemente associada a perfis genéticos de maior risco.31-33
A MASLD é definida histologicamente pela presença de esteatose hepática em mais de 5% dos hepatócitos, na ausência de consumo significativo de álcool (<20 g/dia em mulheres e <30 g/dia em homens). Seu espectro clínico abrange desde a esteatose simples até a MASH, caracterizada por inflamação lobular, balonização hepatocitária e fibrose, podendo evoluir para cirrose e CHC.30
Além do impacto clínico, a MASLD impõe um elevado ônus econômico. Nos Estados Unidos, os custos anuais relacionados à doença ultrapassam US$ 100 bilhões, concentrando-se principalmente nos casos de MASH e de suas complicações. Em estudo multicêntrico recente conduzido por Younossi et al., 34 envolvendo nove países, incluindo o Brasil, estimou-se que os custos médicos diretos anuais associados à MASH avançada (fibrose F3, cirrose compensada e descompensada, CHC e transplante hepático) aumentarão em ≥20% em todos os países e dobrarão até 2040. No Brasil, projeta-se um aumento desses custos de US$ 3,41 bilhões em 2021 para US$ 9,81 bilhões.34
O diagnóstico precoce da MASLD é fundamental no contexto da SMetab, uma vez que ambas compartilham mecanismos fisiopatológicos centrais, como resistência à insulina, inflamação crônica de baixo grau, dislipidemia e disfunção adipocitária.29,30 A MASLD é frequentemente assintomática em suas fases iniciais, o que favorece o subdiagnóstico e o atraso na implementação de medidas terapêuticas, o que permite a progressão silenciosa para fibrose avançada, cirrose e carcinoma hepatocelular. 29,35 Indivíduos com a SMetab apresentam risco significativamente maior de desenvolver formas graves da MASLD, incluindo MASH, fortemente associada à progressão da fibrose hepática e à mortalidade hepática e cardiovascular.27 Assim, o diagnóstico precoce permite a adoção de intervenções oportunas, como mudanças no estilo de vida, controle rigoroso de fatores cardiometabólicos e estratificação de risco para fibrose hepática, estratégias que podem retardar ou até reverter a progressão da doença. Mais ainda, a detecção precoce possibilita o uso de métodos não invasivos para avaliação da fibrose, otimizando o encaminhamento para atenção especializada, reduzindo a necessidade de biópsia hepática e contribuindo para a mitigação do impacto clínico e econômico da MASLD.29,30,35
Fisiopatologia Resumida de Pré DM, DM2 e MASLD
Pré-diabetes e DM2 representam um continuum fisiopatológico que decorre da combinação de resistência à insulina e de disfunção progressiva das células β, em diferentes graus, determinando a gravidade da alteração glicêmica.36 Na compreensão da sua fisiopatologia, é importante reconhecer a relação entre o DM2 e outras condições, como obesidade, SMetab, MASLD, doenças cardiovasculares e renais, visto que todas têm em comum um fator causal: a adiposopatia.37
Há uma interação complexa entre a disfunção do tecido adiposo, a RI e a inflamação crônica, que contribuem para o desenvolvimento do DM2 e para desfechos cardiovasculares e renais. A adiposopatia, definida como a disfunção patológica do tecido adiposo, está associada à incapacidade do tecido adiposo de expandir-se adequadamente, levando ao acúmulo de gordura em órgãos como fígado, músculo, pâncreas, coração e rins. O tecido adiposo ectópico promove aumento na liberação de ácidos graxos livres e de adipocinas pró-inflamatórias, como TNF-α e IL-6, que contribuem para a RI, dificultando ainda mais a captação e a utilização da glicose.37 Além disso, o acúmulo ectópico de gordura promove RI nos tecidos e órgãos-alvo, mantendo-se em um ciclo vicioso, agravado por uma ação lipotóxica, com inflamação e fibrose, o que causa disfunção de cada um destes órgãos.37,38 Dessa forma, um grupo brasileiro propôs recentemente uma definição mais abrangente da SMetab — CARDIAL-MS (CardioRenalDiabetes and Liver- Metabolic Syndrome) — que integra a SMetab à MASLD, enfatizando a interconexão entre obesidade, DM2 e doenças cardiovasculares e renais37. O modelo sugere quatro estágios progressivos que ajudam na identificação de pacientes em risco:
- Ganho de peso e disfunção do tecido adiposo (distribuição de gordura desfavorável: aumento da RCQ, RCAlt, FMR, evidência de gordura ectópica)
- Presença de fatores e marcadores metabólicos de risco envolvendo um ou mais dos órgãos em questão (Ex. esteatose, albuminúria, DCVA subclínica)
- Presença de doenças metabólicas, cardíacas, renais e hepáticas em estágios
- Doença avançada cardio-renal-hepática-metabólica.
RCQ= razão cintura-quadril, RCAlt= razão cintura-altura, DCVA= doença cardiovascular aterosclerótica
A fisiopatologia do DM2 não difere muito daquela do pré-diabetes. Entretanto, deve-se considerar que há alguns subtipos de diabetes do adulto, em geral rotulados como DM2 quando se exclui o diabetes autoimune do adulto (LADA).38,39 O DM2 apresenta uma arquitetura genética altamente poligênica, com mais de 1.000 variantes identificadas até o momento.40 Algumas das variantes mais relevantes incluem TCF7L2, PPARG, KCNJ11, CDKAL1, SLC30A8, HHEX, MTNR1B, GCK
e IRS1. Para o contexto desta monografia, é importante destacar algumas associadas a RI, à distribuição da gordura corporal e à MASLD, como PPARG, IRS1, GRB14 e ARL15.40
Em especial, na fisiopatologia do DM2, deve-se realçar o papel do fígado e a interação do novo eixo fígado-células α pancreáticas (cels-α) recentemente descrito.37,41-43 Resumidamente, o excesso de gordura depositada no fígado induz resistência ao efeito do glucagon no metabolismo dos aminoácidos, mas não no da glicose. Os aminoácidos tendem a se acumular na circulação e, em um mecanismo de feedback recentemente desvendado,41,42 estimulam as células α a produzirem mais glucagon e, com isso, maior produção hepática de glicose (Fig. 1). Este modelo fisiopatológico está em consonância com a “Twin-cycle hypothesis” de Roy Taylor, que envolve o fígado e o pâncreas num ciclo de esteatose hepática e pancreática que leva à disfunção destes órgãos e se que se reforçam mutualmente.43
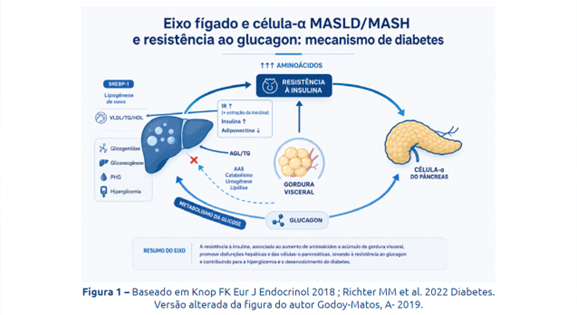
MASLD/MASH
A MASLD é uma doença complexa, caracterizada pelo acúmulo de lipídios no fígado e pelo potencial de progressão para MASH, fibrose e cirrose. Apenas 20–30% dos indivíduos evoluem para formas avançadas, o que reflete a interação entre fatores genéticos e ambientais. Como já discutido anteriormente, a adiposopatia e o complexo metabólico de RI no tecido adiposo e no músculo, permitem o aumento dos AGLs circulantes que se acumulam no fígado, levando a esteatose, lipotoxicidade e inflamação. A hiperinsulinemia resultante estimula a lipogênese hepática de novo. Em conjunto, há liberação de citocinas pró-inflamatórias (leptina, resistina), redução de adiponectina, estresse oxidativo, ativação de JNK e apoptose hepatocitária. A microbiota intestinal disbiótica contribui para a inflamação hepática por meio do aumento da
permeabilidade intestinal, da translocação bacteriana, da ativação de receptores Toll-like e da maior produção de AGLs, estimulando IL-6 e TNF-α. Alterações nos receptores nucleares, especialmente o PPAR-α, reduzem o catabolismo de lipídios e correlacionam-se com a gravidade histológica da doença. Fatores genéticos modulam a susceptibilidade à esteatose, fibrose, cirrose e carcinoma hepatocelular, reforçando a importância de compreender os gatilhos patogênicos para a elaboração de estratégias diagnósticas e terapêuticas. O eixo central da progressão MASLD–MASH envolve a fibrogênese hepática e integra disfunção metabólica, inflamação sistêmica, lipotoxicidade e determinantes genéticos.39-42
- Benefícios do Tratamento de Pré-DM, DM2 e MASLD/MASH com Pioglitazona.
Benefício Glicêmico
O estudo ACT NOW,7 buscou responder se a pioglitazona poderia prevenir a evolução para DM2. Foram randomizados 602 pacientes com intolerância à glicose, em duplo-cego, e controlados com placebo. A mediana de acompanhamento foi de 2,4 anos e, nesse período, a taxa de evolução para DM2 foi de 2,1% com pioglitazona e 7,6% com placebo [HR 0,28 (IC 95%: 0,16 a 0,49); P<0,001]. Outros benefícios também foram importantes. A taxa de conversão para normoglicemia foi maior com a pioglitazona (48% vs 28 %) e houve, como esperado, melhora da sensibilidade à insulina, mas também redução da pressão arterial diastólica, aumento dos níveis de HDL-C e redução dos níveis de triglicerídeos.7
No tocante ao tratamento do DM2, a pioglitazona tem demonstrado ser um potente e eficaz agente antidiabético. Uma recente revisão sistemática e meta-análise,44 avaliou a eficácia e segurança da monoterapia com pioglitazona em comparação com outros medicamentos antidiabéticos orais em pacientes com DM2. Foram analisados 16 ensaios clínicos randomizados, envolvendo 2.681 participantes, publicados entre 2002 e 2017. A pioglitazona apresentou eficácia semelhante à dos comparadores na redução da HbA1c [0,05% (95% IC:
−0,21 a 0,11)] e maior eficácia na redução da glicemia de jejum [0,24 mmol/l (95% IC: −0,48 a
−0,01)]. Além disso, mostrou efeitos positivos no perfil lipídico, reduzindo os triglicerídeos e aumentando o HDL. Também contribuiu para a redução da pressão arterial, embora sem significância estatística. Quanto à segurança, observou-se aumento significativo de edema dos membros inferiores, maior risco de IC, e não houve evidências de aumento do risco de câncer de bexiga (discutido adiante).44 Em conclusão:
- A pioglitazona é uma opção eficaz no tratamento do DM2, especialmente em pacientes com resistência à insulina, dislipidemia, hipertensão ou histórico de doenças
- Apesar de seus benefícios, os efeitos adversos, como ganho de peso e edema, devem ser monitorados, especialmente em pacientes com insuficiência cardíaca.
- A pioglitazona pode ser usada como alternativa à metformina ou, quando necessário, em combinação com outros medicamentos.
O estudo conclui que a pioglitazona apresenta um balanço favorável entre riscos e benefícios, sendo uma opção viável para o manejo do DM2, especialmente em pacientes com fatores de risco cardiovascular.44
Benefícios na MASLD/MASH/Fibrose
Estudos clínicos, como o PIVENS45, incluíram pacientes com IMC médio de ~35 kg/m², circunferência abdominal de 107–109 cm e percentual de gordura de ~40%, demonstrando que a pioglitazona reduz significativamente a esteatose e a inflamação hepática, com efeitos comparáveis à vitamina E quanto à resolução histológica.45
Em um estudo multicêntrico brasileiro, retrospectivo,46 com 65 pacientes tratados com pioglitazona 30–45 mg/dia por até 10 anos, observou-se redução significativa de ALT e GGT em todos os pacientes; diminuição do CAP (esteatose) em pacientes tratados por 4–10 anos (p = 0,002), indicando redução de esteatose hepática; melhora nos escores FAST™, avaliando rigidez hepática e inflamação, tanto em 1–3 anos (p = 0,042) quanto em 4–10 anos (p = 0,012).46
Uma meta-análise de 8 estudos com TZDs, incluindo pacientes com e sem DM2, demonstrou redução da fibrose avançada (OR: 3,15) e possível resolução da MASLD (OR: 3,22), com efeitos significativos restritos à pioglitazona, independentemente da presença de DM2.47
Uma outra meta-análise de 48 ECRs (n = 2.356), em rede, avaliou diferentes intervenções para esteatohepatite, incluindo medicamentos e cirurgia bariátrica.48 A pioglitazona apresentou o maior efeito na redução do escore NAS por semestre (-1,50; IC 95%: -2,08 a -1,00), sendo também a melhor intervenção para reduzir a esteatose e a inflamação lobular, seguida pelo bypass gástrico em Y de Roux (RYGB) (-1,00; IC 95%: -1,70 a -0,32).48
- Benefício no tratamento de pré-DM em relação às demais drogas disponíveis.
Entre os principais estudos que demonstram o benefício da pioglitazona em pacientes com pré- diabetes, destaca-se o IRIS. Neste estudo prospectivo, com 3.876 adultos com evento cerebrovascular isquêmico prévio e resistência à insulina, o uso da pioglitazona nas doses de 30 e 45 mg, por um período médio de 4,8 anos, reduziu a incidência de DM2 em 52% em comparação com o placebo. Dessa forma, embora a prioridade em relação ao tratamento do pré- diabetes seja pela metformina, existe a recomendação da American Diabetes Association, para que a pioglitazona seja considerada em pacientes com história de acidente vascular cerebral (AVC) que tenham evidências de resistência à insulina e pré-diabetes, com o objetivo de reduzir o risco de um novo evento cardiovascular.49
Considerando a eficácia da pioglitazona em relação aos outros tratamentos para pré-diabetes, uma metanálise avaliou três estudos que compararam a eficácia da pioglitazona em relação à metformina. Foram selecionados apenas estudos randomizados e controlados com duração mínima de 24 semanas. A incidência de DM2 foi de 9 em 168 participantes no grupo de pioglitazona, em comparação com 9 em 163 participantes em uso de metformina (razão de risco
de 0,98; IC 95%: 0,40–2,38). Assim, a pioglitazona não demonstrou inferioridade à metformina na redução da incidência de DM2.50
Embora não existam estudos publicados que comparem diretamente a eficácia da pioglitazona aos inibidores da dipeptidil peptidase 4 (DPP-4) em pacientes com pré-diabetes, não há evidências robustas de seu uso para prevenção do diabetes em pré-diabetes, nem recomendações formais das principais sociedades para essa indicação. Segundo a diretriz de tratamento de pré-diabetes da Sociedade Brasileira de Diabetes (SBD), os inibidores do iSGLT2 e os inibidores da DPP-4 não são considerados para a prevenção do DM2, por falta de evidências.15
Mais recentemente, em relação aos iSGLT2, uma meta-análise de estudos randomizados incluiu pacientes com HbA1c < 6,5%, classificados como pré-diabéticos ou normoglicêmicos, e divididos em grupos tratados com dapagliflozina ou placebo.51 Nos estudos avaliando pacientes com insuficiência cardíaca, houve redução de 33% na incidência de novos casos de DM2 com dapagliflozina em comparação com placebo. Em sete estudos que avaliaram pacientes com doenças cardiovasculares e renais, a incidência de DM2 foi reduzida em 26% no grupo tratado com dapagliflozina. Embora essa meta-análise possa oferecer uma nova possibilidade terapêutica, não há estudos comparativos entre iSGLT2 e pioglitazona, nem recomendações formais para o uso de iSGLT2 no tratamento do pré-diabetes.51
Em relação às terapias baseadas no agonista de GLP-1, não há recomendação específica para o tratamento do pré-diabetes; porém, reconhece-se a importância do tratamento do sobrepeso e da obesidade para prevenir o DM2. Não existem estudos comparando essas terapias com a pioglitazona no contexto do tratamento do pré-diabetes; porém, há comparações quanto a desfechos hepáticos e cardiovasculares, que serão detalhadas no tópico “Benefício Cardiovascular”.49, 52
- Benefício Cardiovascular.
Segundo o Standards of Care da American Diabetes Association, publicado em 2026, o uso de pioglitazona deve ser considerado para reduzir o risco de AVC ou IAM em pessoas com história prévia de AVC, resistência à insulina e pré-diabetes. Essa recomendação tem origem no estudo IRIS (Insulin Resistance Intervention after Stroke)53, que avaliou pessoas com história recente de AVC ou de ataque isquêmico transitório (AIT). Os pacientes não tinham diagnóstico de DM2, mas apresentavam resistência à insulina, definida por HOMA-IR > 3, e foram acompanhados por 4,8 anos, recebendo pioglitazona de 30 a 45 mg ou placebo. 49,53
No fim desse período, o desfecho primário (AVC ou IAM fatal ou não fatal) ocorreu em 175 de 1939 pacientes (9%) no grupo pioglitazona e em 228 de 1937 (11,8%) no grupo placebo. Da mesma forma, quanto ao desenvolvimento de diabetes, houve diagnóstico de DM2 em 73 (3,8%) no grupo da pioglitazona, enquanto em 149 (7,7%) no grupo placebo. Assim, o estudo mostrou menor risco de AVC e IAM, bem como menor risco de evolução para DM2, nesse subgrupo de pacientes com resistência à insulina e AVC prévio.53
Outro estudo mostra benefícios na prevenção secundária de doenças cardiovasculares. A meta- análise de Zhou et al.54 teve como objetivo avaliar o efeito da pioglitazona na prevenção primária e secundária de doenças cardiovasculares e na redução de eventos adversos renais em pacientes com DM2 ou com alto risco de DM2. O estudo demonstrou que a pioglitazona reduz o risco de eventos cardiovasculares maiores (infarto não fatal, AVC não fatal e morte cardiovascular) em pacientes com histórico de doença cardiovascular estabelecida (RR 0,8; IC 95% 0,7–0,9), com benefício principalmente em infarto do miocárdio e AVC não fatal, mas sem efeito sobre mortalidade cardiovascular. Além disso, houve redução da albuminúria nos pacientes em uso da pioglitazona.54
Confirmando os dados de prevenção secundária e trazendo novos dados sobre a prevenção primária de doenças cardiovasculares, um estudo conduziu um ensaio clínico emulado, com base em dados eletrônicos de coorte de todo o território de Hong Kong.52 Teve como objetivo estimar os efeitos causais de agonistas de GLP-1 e de pioglitazona sobre os riscos de eventos adversos cardiovasculares e hepáticos graves em pacientes com DM2. Um total de 8.922 pacientes foi incluído, divididos igualmente (4.461 cada) entre novos usuários de agonistas do receptor de GLP-1 (GLP-1RA) e de pioglitazona. As medianas de IMC nos grupos foram de 30,1 kg/m² e 29,4 kg/m² para GLP-1RA e pioglitazona respectivamente. Para a HbA1c (hemoglobina glicada) a mediana foi de 8,4% para ambos os grupos. A maioria dos pacientes não apresentava eventos cardiovasculares prévios. Por fim, o estudo mostrou riscos semelhantes de desfechos cardiovasculares (razão de risco 0.99; 95% CI 0.80–1.22) e hepáticos (razão de risco 0.94; 95% CI 0.66–1.34). No entanto, o grupo em uso de análogos de GLP-1 apresentou menor risco de insuficiência cardíaca do que o grupo tratado com pioglitazona (razão de risco de 0.65; 95% CI: 0.51–0.83).52
Quebrando Objeções:
-Câncer de Bexiga
No estudo PROactive,55 entre os eventos adversos, observou-se um desequilíbrio não significativo em novos casos de câncer de bexiga: 14 (1%) no grupo pioglitazona e 6 (1%) no grupo controle (p = 0,069). Este achado abriu uma intensa discussão na literatura, que perdura até os dias atuais, com resultados conflitantes.56 Após o término do estudo PROactive, uma análise pré-especificada de 6 anos de seguimento dos pacientes que o concluíram revelou que o desequilíbrio desapareceu.57 Assim, no período combinado de fase de estudo e de observação, com média de 8,7 anos, havia menos casos de câncer de bexiga no grupo pioglitazona do que no grupo controle, 15 (0,6%) vs 19 (0,7%), se excluídos os primeiros 365 dias. Não houve diferença no diagnóstico de quaisquer outras malignidades (RR=1.05, 95% IC 0.89 a 1.2) nem na malignidade da bexiga. (RR=1.06, IC 95% 0.59 a 1.89).57 Isto se confirmou na análise pré- especificada de 10 anos de acompanhamento.58 A incidência de malignidade total foi similar entre os grupos, e a de câncer de bexiga foi relatado em 0,8% dos pacientes (n = 14) do grupo da pioglitazona vs 1,2% (n = 21) no grupo placebo (RR 0,65; 95% IC 0,33–1,28).58
O estudo Kaiser Permanent Northern California (KPNC)59
Com as incertezas quanto ao risco de malignidade na bexiga, a agência reguladora Food and Drug Administration (FDA) nos Estados Unidos e o manufaturador da pioglitazona, concordaram em estabelecer um estudo observacional do tipo coorte e caso-controle, com duração de 10 anos. Abaixo, o resumo dos principais achados:
- Foram analisados dados de 099 pessoas com diabetes entre 1997 e 2012 dos quais
34.181 (18%) dos participantes usaram pioglitazona, com duração média de 2,8 anos.
- A incidência de câncer de bexiga foi de 89,8 por 000 pessoas-ano entre usuários da pioglitazona, comparado a 75,9 entre não usuários.
- O uso de pioglitazona não mostrou associação significativa com o risco de câncer de bexiga (HR ajustado: 1,06; IC 95%: 0,89-1,26).
- A análise de 10 tipos adicionais de câncer, pré-estabelecida, incluiu 507 pessoas e o uso de pioglitazona foi associado a um aumento do risco de câncer de próstata (HR: 1,13; IC 95%: 1,02-1,26) e de câncer de pâncreas (HR: 1,41; IC 95%: 1,16-1,71).
Uma forma importante de analisar a associação entre um determinado medicamento e possíveis eventos adversos sérios é observar se há relação entre a dose cumulativa do medicamento e o risco a ser avaliado. No caso do estudo KPNC, observou-se o seguinte:
- Dose cumulativa de 1–14.000 mg: Incidência de câncer de bexiga de 69,1 por 000 pessoas-ano. HR ajustado: 0,90 (IC 95%, 0,69-1,16).
- Dose cumulativa de 001–40.000 mg: Incidência de câncer de bexiga de 96,9 por
100.000 pessoas-ano. HR ajustado: 1,10 (IC 95%, 0,85-1,42).
- Dose cumulativa acima de 000 mg: Incidência de câncer de bexiga de 101,4 por
100.000 pessoas-ano. HR ajustado: 1,07 (IC 95%, 0,79-1,44).
Os resultados não mostraram associação estatisticamente significativa entre o risco de câncer de bexiga e a dose cumulativa de pioglitazona. Além disso, os testes de tendência linear para dose cumulativa não foram estatisticamente significativos (P = 0,64). Em conclusão, o estudo constatou que não há aumento estatisticamente significativo no risco de câncer de bexiga associado ao uso de pioglitazona, em contraste com análises anteriores. Também sugere que o aumento do risco de câncer de próstata e de pâncreas pode ser devido a fatores de confusão ou à causalidade reversa.
Baddam et al.56 publicaram recentemente uma revisão sistemática, na qual analisaram 212 artigos iniciais, dos quais 176 foram excluídos por não atenderem aos critérios de inclusão, 24 por dados inadequados e 6 por inacessibilidade, resultando em 6 estudos elegíveis para a revisão. Entre estes estudos, apenas 2 confirmaram a associação entre pioglitazona e câncer de bexiga, enquanto 4 não a confirmaram.56 Assim, após mais de 20 anos sob escrutínio e apesar de alguns estudos conflitantes, não parece que a associação entre a pioglitazona e o câncer de bexiga tenha sido comprovada.
-Doenças cardíacas.
Apesar de estudos demonstrarem benefícios, principalmente na prevenção secundária, a pioglitazona pode aumentar o risco de descompensação de insuficiência cardíaca. O mecanismo da descompensação parece estar relacionado à retenção hídrica, sem evidências que suscitem a suspeita de toxicidade miocárdica. A diretriz europeia de prevenção de doenças cardiovasculares indica que a pioglitazona deve ser considerada em pacientes com DM2 e história de doenças cardiovasculares sem diagnóstico de insuficiência cardíaca.60 A metanálise de Zhou Y et al., citada anteriormente,54 que mostrou benefícios na prevenção primária, avaliou
13 estudos com um total de 15.231 participantes, nos quais foram relatados casos de hospitalização por insuficiência cardíaca, de morte cardiovascular e de mortalidade por todas as causas. O estudo mostrou que houve um risco 33% maior de hospitalização por insuficiência cardíaca no grupo de pioglitazona (RR 1,3; IC 95% 1,1–1,6) em relação ao grupo controle (composto por placebo ou tratamento usual). No entanto, é importante notar que não houve diferença na mortalidade por todas as causas (RR 1,0; IC 95% 0,8–1,1) nem no risco de morte de origem cardiovascular (RR 1,0; IC 95% 0,7–1,2)54.
Dessa forma, a pioglitazona reduz eventos cardiovasculares não fatais (infarto e AVC) em pacientes com doença cardiovascular estabelecida, mas aumenta o risco de hospitalização por insuficiência cardíaca. Esses achados reforçam a ideia de que o benefício da pioglitazona deve ser ponderado em pacientes com risco de descompensação cardíaca.54 Na prática, há contraindicação ao início da pioglitazona em pacientes com insuficiência cardíaca estabelecida nas classes III ou IV da New York Heart Association (NYHA). Quando há insuficiência cardíaca nas classes funcionais NYHA I e II, a pioglitazona pode ser indicada com cautela e em menor dose (Bula Americana da pioglitazona). 61
É interessante entender se a IC ocorre em função de, ou por causa de, um aumento da retenção hídrica e se os pacientes já tinham algum grau de IC, assintomáticos ou oligossintomáticos, e, portanto, a pioglitazona apenas “descobriu-a”. Um estudo mecanístico buscou entender qual seria o efeito dessa medicação sobre a dinâmica cardíaca. Doze indivíduos com TDM e 12 com tolerância normal à glicose foram submetidos a um clamp insulinêmico euglicêmico e a exames de imagem — ressonância magnética cardíaca (RMC) para avaliar a função do VE e tomografia por emissão de pósitrons (PET) para medir a captação de glicose e a perfusão miocárdica.62 O tratamento com pioglitazona reduziu a HbA1c em 0,9% e melhorou a pressão arterial sistólica e diastólica. A captação de glicose miocárdica aumentou em 75% e a perfusão miocárdica, em 16%. A função diastólica do VE melhorou, com aumento significativo da razão E/A e da taxa de enchimento do VE. A fração de ejeção e o volume de ejeção sistólica também aumentaram significativamente.62
O mesmo grupo demonstrou, num estudo posterior de 24 meses de duração, que a gordura epicárdica (GE) e a gordura paracárdica (GP), quantificadas por RMC, diminuíram em 9% (p < 0,01 para GE e p = 0,09 para GP). A função diastólica melhorou com aumento do fluxo E/A e do fluxo ventricular esquerdo máximo (FVEM) após o tratamento (p < 0,05).63 Os resultados também demonstram que a redução da GE está correlacionada com a melhora na sensibilidade à insulina, medida pelo método padrão-ouro de clamp euglicêmico de insulina; as melhorias na função diastólica do ventrículo esquerdo (E/A e PLVFR), mediadas pela pioglitazona, estão intimamente relacionadas à redução da GE após o tratamento com pioglitazona em pacientes com DM2 sem doença cardiovascular clínica.63
- Doenças óssea (Risco-benefício).
A associação entre DM2 e osteoporose é descrita na literatura com base no risco aumentado de fraturas nessa população. Entre os fatores metabólicos envolvidos na fisiopatologia da osteoporose relacionada ao DM2 estão: obesidade, hiperglicemia e os produtos finais de glicação avançada (AGEs). A obesidade cursa com estado inflamatório e elevação dos níveis de interleucina-6 e do fator de necrose tumoral alfa, que ativam a via do RANK, com consequente estímulo aos osteoclastos e à reabsorção óssea.64
A hiperglicemia suprime a maturação e a diferenciação de osteoblastos, com redução da formação óssea, enquanto os AGEs, como produto da própria hiperglicemia e do estresse oxidativo, levam a alterações estruturais do colágeno, inibem a proliferação e estimulam a apoptose de osteoblastos.64,65 Dessa forma, uma metanálise mostrou que um aumento de 1% na hemoglobina glicada (HbA1c) aumenta o risco de fraturas em 8%, e esse risco aumenta com o tempo prolongado de descontrole glicêmico, assim como com episódios de hipoglicemias graves.66 O risco de quedas, além de estar associado aos episódios de hipoglicemias, também se manifesta com maior frequência em pacientes com neuropatia e retinopatia diabéticas.64
Segundo o Standards of Care da American Diabetes Association, publicado em 2026, recomenda-se a realização de DXA em pessoas com diabetes a partir dos 65 anos ou, em caso de múltiplos fatores de risco para fratura, a partir dos 50 anos. Entre os fatores de risco incluem- se: hipoglicemias ou quedas frequentes, tempo de diagnóstico de mais de 10 anos, HbA1c maior que 8%, complicações relacionadas ao DM (neuropatia, retinopatia e doença renal do diabetes), uso de glicocorticoides, medicamentos associados a maior risco de fraturas (insulina, sulfonilureias, pioglitazona).66
A pioglitazona, por atuar como agonista do PPAR-y, tem a capacidade de estimular a diferenciação de células-tronco mesenquimais em adipócitos na medula óssea, o que leva a um desvio na formação de osteoblastos. Logo, o estímulo ao PPAR-y reduz a formação óssea e pode aumentar a predisposição a fraturas.65
Um estudo de banco de dados, com 206.672 participantes com DM2, avaliou o efeito cumulativo do uso de pioglitazona sobre o risco de fraturas de quadril. Apesar de estudos iniciais terem mostrado impacto da pioglitazona apenas no risco de fraturas distais em mulheres, esse estudo evidenciou aumento do risco de fraturas de quadril em homens e mulheres, em associação ao efeito cumulativo da pioglitazona.67 Outros tratamentos também, como as sulfonilureias e insulinoterapia, têm relação com maior risco de fraturas, o que provavelmente se relaciona ao maior risco de hipoglicemia desses medicamentos.66
Na prática, há variabilidade no risco de fratura entre pacientes com DM2, o que parece decorrer de diferentes fenótipos clínicos dessa condição. Essa diferença possivelmente reflete diferentes fatores que contribuem para o prejuízo da qualidade óssea, como tempo de diabetes, pior controle glicêmico e tratamentos instituídos.64
Por fim, é importante destacar que o maior risco de fraturas é um efeito adverso descrito no uso de pioglitazona; porém, a osteoporose não é uma contraindicação absoluta para o uso de pioglitazona. Dessa forma, torna-se necessário avaliar a relação risco-benefício em cada paciente, considerando os fatores associados ao risco de fratura, bem como os possíveis benefícios da indicação da pioglitazona. Caso seja considerado o uso da pioglitazona em pacientes com osteopenia ou osteoporose, indica-se a implementação de medidas para reduzir o risco de fraturas.66
Ganho de peso (paradoxo do ganho de peso bom:
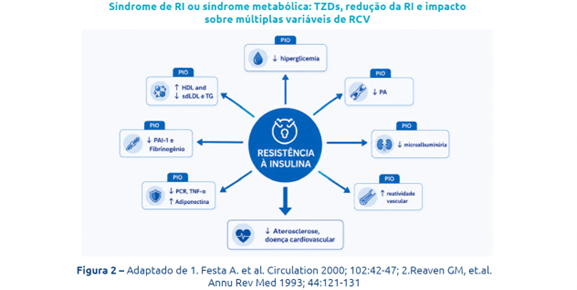
É, no mínimo, curioso e paradoxal que pacientes sob uso de TZDs ganhem peso, mas, ao mesmo tempo, melhorem o controle glicêmico, reduzam a RI, reduzam a gordura visceral, melhorem o perfil lipídico e obtenham diversos outros benefícios cardiometabólicos (Fig. 2). Esta, sem dúvida, é a única situação em biologia, até onde conhecemos, em que isso ocorre. A explicação mais razoável é que há redistribuição da gordura corporal, favorecendo a adipogênese e o depósito na gordura subcutânea periférica (nas pernas e na região glútea). Pelo menos 2 estudos experimentais demonstraram claramente esse fenômeno.67,68 Em ambos, a pioglitazona aumentou o peso corporal, mas o aumento ocorreu principalmente nos membros inferiores. No estudo de White et al.,68 observou-se uma redução da gordura visceral e um aumento significativo na formação de novos adipócitos no depósito femoral subcutâneo [(scFEM) Δ = 3,3 ± 1,6%; p = 0,04], mas não no depósito abdominal subcutâneo [(scABD) Δ = 2,0 ± 2,1%; p = 0,32]. Estes resultados mostram que, embora tenha havido ganho de peso, houve redistribuição de gordura, favorecendo o depósito no scFEM, mais saudável metabolicamente.
Como já discutido acima, no estudo seminal de Gastaldelli et al.,14 além da melhora na SI, a melhora na função da célula β e o consequente aumento na secreção de insulina correlacionaram-se positivamente com o aumento do peso corporal, da massa de gordura e da taxa de desaparecimento da glicose (Rd)14. Embora possa parecer paradoxal, esse é um dos mecanismos de ação do medicamento e certamente um efeito desejável.
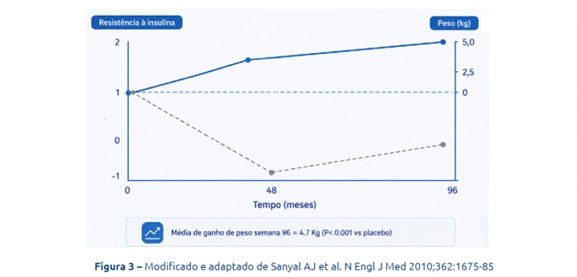
Outro exemplo, no estudo PIVENS45, em pacientes com MASH, comparando pioglitazona e vitamina E versus placebo, o grupo da pioglitazona foi o único a apresentar ganho significativo de peso (aumento médio de 4,7 kg, P<0,001 em comparação com placebo). Entretanto, o grupo da pioglitazona apresentou uma melhora significativa na resistência à insulina 45 (Fig 3). Assim, podemos dizer que esse é um ganho de “peso bom”. Por suposto, alguns pacientes também podem apresentar retenção hídrica (discutida noutra parte desta monografia), o que contribui para um aumento de peso não associado ao aumento da gordura periférica.
O que avaliar antes de iniciar a pioglitazona (Guia prático de indicações e contraindicações).
Apesar da extrema importância do conhecimento sobre a farmacologia do medicamento e a fisiopatologia do pré-diabetes, DM2 e da MASLD, o foco na hora da decisão terapêutica deve ser no paciente. O conceito de terapia centrada no paciente vem sendo abordado nas últimas diretrizes sobre o tratamento do diabetes.66 Então, na prática, quais pacientes mais se beneficiarão da pioglitazona? Quais fatores precisamos avaliar para identificar esse paciente? E quais pacientes não devem usar a pioglitazona?
A partir do conceito de terapia centrada no paciente, precisaremos avaliar os seguintes fatores, segundo o ADA Comprehensive Medical Evaluation and Assessment.66
- Quais são as condições associadas e as complicações do DM2, bem como o estado geral do paciente?
- Qual a meta de HbA1c, considerando idade, funcionalidade, cognição, expectativa de vida, risco de hipoglicemia e fragilidade?
- Qual é o peso e o risco cardiovascular?
- Quais são as condições socioeconômicas e a disponibilidade financeira para o tratamento?
- Quais são as preferências do paciente em relação às opções de tratamento?
Segundo a diretriz da SBD, é recomendado que todos os adultos com DM2 sejam avaliados quanto ao risco cardiovascular, ao índice de massa corporal, à HbA1c e à função renal antes de definir a estratégia terapêutica e o uso de agentes antidiabéticos. Dessa forma, com base no perfil de doença cardiovascular, embora a prioridade nas diretrizes seja o uso de iSGLT2 e análogos de GLP-1, com o objetivo de reduzir o RCV, é importante lembrar o papel da pioglitazona na redução do risco. Além disso, dado que a condição socioeconômica pode, muitas vezes, limitar a indicação de análogos de GLP-1 e/ou de iSGLT2, a pioglitazona é mais acessível e é uma das 3 classes de medicamentos com confirmação para a redução de RCV (tratamento DM2, SBD).4,60
Além do risco cardiovascular, o rastreio e a definição da gravidade da MASLD também devem influenciar a escolha do tratamento do DM2 e do pré-diabetes. Além das evidências sobre o uso da pioglitazona no tratamento da MASLD descritas acima, a diretriz da SBD recomenda a indicação da pioglitazona como tratamento de primeira linha para esteato-hepatite e/ou fibrose em pessoas com DM2.4,8 Da mesma forma, nos standards of care da ADA 2026, indica-se a Diante desse perfil de pacientes que teriam maior benefício do uso da pioglitazona, o próximo passo seria avaliar a presença de fatores que pudessem contraindicar o seu uso. Dessa forma, pode ser necessária a realização da densitometria óssea e a avaliação sobre o risco de fraturas, e avaliar criteriosamente o risco de IC. Em pacientes com IC estabelecida, classes III ou IV do New York Heart Association (NYHA), o uso de pioglitazona é contraindicado. 61 Não obstante,
nos casos de IC nas classes funcionais I e II, bem como em pacientes com osteoporose estabelecida, a pioglitazona pode ser indicada com cautela, considerando-se o início em menor dose.49,61 Da mesma forma, a pioglitazona está contraindicada em pacientes com história de câncer de bexiga ativo, embora a associação entre o uso desse medicamento e maior incidência de malignidade não tenha sido claramente estabelecida.
Finalmente, a pioglitazona mantém-se como o único sensibilizador da ação da insulina, com benefícios bem estabelecidos no controle glicêmico, na resolução da MASH e na fibrose hepática, na prevenção do diabetes e de desfechos cardiovasculares. Em pelo menos dois estudos, preveniu o diabetes em pacientes com pré-diabetes e foi o primeiro medicamento antidiabético a reduzir o risco de diabetes e, ao mesmo tempo, reduzir desfechos cardiovasculares em um mesmo ensaio clínico.69
O quadro abaixo sugere as principais razões para o uso da pioglitazona no tratamento dos pacientes elegíveis:
As muitas razões para a pioglitazona:
- A RI é um mecanismo fisiopatológico para DM2 e DCVA
- A pioglitazona é o único sensibilizador da insulina restante
- Preservação e melhora da função de células-β
- Eficácia no controle da glicose e na prevenção do (estudos ACT NOW e IRIS)
- Pode ser combinado com a maioria dos AD
- Alveja vários processos metabólicos e inflamatórios (perfil lipídico, TNF-α, adiponectina, PCR, disfunção endotelial...)
- Não associada à hipoglicemia
- Primeira linha para tratamento da MASH em algumas diretrizes
- Favorável em desfechos CV substitutos (PERISCOPE, CHICAGO)
- ERCs mostrando redução de desfechos CV maiores (ProACTIVE, IRIS)
- Meta-análise dos ERCs: redução nos desfechos CV
- Efeitos adversos bem conhecidos (IC e fraturas)
- É o AD mais escrutinizado entre todos
- Razão risco/benefícios favorável
- Ganho de peso é efeito desejável (redistribuição da gordura em favor da gordura nas pernas)
- Menor mortalidade CV e por todas as causas (estudos observacionais)
- Pioglitazona não tem mais segredos!
AD- antidiabético; DCVA- doença cardiovascular aterosclerótica; ERC-Estudo randomizado e controlado;
Referências:
- Yki-Jarvinen, Thiazolidinediones. N Engl J Med 2004;351:1106-18.
- Eldor R, DeFronzo RA, Abdul-Ghani M. In Vivo Actions of Peroxisome Proliferator–Activated Receptors: Glycemic control, insulin sensitivity, and insulin Diabetes Care. 2013; August 36 (Supplement_2): S162–S174. https://doi.org/10.2337/dcS13-2003
- Choi SS, Park J, Choi Revisiting PPARγ as a target for the treatment of metabolic disorders. BMB Rep. 2014 Nov;47(11):599-608. doi:10.5483/bmbrep.2014.47.11.174. PMID: 25154720; PMCID: PMC4281338.
- Lyra R, Valente F, Albuquerque L, Cavalcanti S, Tambascia M, Silva Júnior WS & Bertoluci Manejo da Terapia Antidiabética no DM2. Diretriz Oficial da Sociedade Brasileira de Diabetes 2025. DOI: 0.29327/5660187.2025-14, ISBN: 978-65-5941-367-6
- American Diabetes Association (ADA): Pharmacologic Approaches to Glycemic Treatment: Standards of Care in Diabetes—2025. Diabetes Care 2025;48(Suppl. 1): S181–S206
- Khan U, Majeed Z, Khan MH, Elsnhory AB, Amin AM, Nawaz A, et Efficacy and Safety of Pioglitazone Add- On in Patients With Type 2 Diabetes Mellitus Inadequately Controlled With Metformin and Dapagliflozin: A Systematic Review and Meta-Analysis of Randomised Controlled Trials. Endocrinol Diab Metabol. 2025, 8(3), e70061. https://doi.org/10.1002/edm2.70061
- DeFronzo RA, Tripathy D, Schwenke DC, Banerji MA, Bray G, Buchanan TA et Pioglitazone for Diabetes Prevention in Impaired Glucose Tolerance. N Engl J Med 2011; 364:1104-1115
- Godoy-Matos AF, Valério CM, Silva Júnior WS, de Araujo-Neto JM, Bertoluci 2024 UPDATE: the Brazilian Diabetes Society position on the management of metabolic dysfunction-associated steatotic liver disease (MASLD) in people with prediabetes or type 2 diabetes. Diabetol Metab Syndr. 2024 Jan 19;16(1):23. doi: 10.1186/s13098-024-01259-2.
- Moreira RO, Valerio CM, Villela-Nogueira CA, Cercato C, Gerchman F, Lottenberg AMP, et al. Brazilian evidence-based guideline for screening, diagnosis, treatment, and follow-up of metabolic dysfunction- associated steatotic liver disease (MASLD) in adult individuals with overweight or obesity: A joint position statement from the Brazilian society of endocrinology and metabolism (SBEM), Brazilian society of hepatology (SBH), and Brazilian association for the study of obesity and metabolic syndrome (Abeso). Arch Endocrinol Metab. 2023;67(6):e230123. h t t p s : / / d o i . o r g / 1 0 . 2 0 9 4 5 / 2 3 5 9 - 4 2 9 2 - 2 0 2 3 - 0 1 2
- Cusi K, Abdelmalek MF, Apovian CM, Balapattabi K, Bannuru RR, Barb D, et al. Metabolic Dysfunction- Associated Steatotic Liver Disease (MASLD) in People With Diabetes: The Need for Screening and Early Intervention. A Consensus Report of the American Diabetes Diabetes Care. 2025 Jul 1;48(7):1057-1082. doi: 10.2337/dci24-0094. PMID: 40434108
- Sakamoto J, Kimura H, Moriyama S, Odaka H, Momose Y, Sugiyama Y et al. Activation of Human Peroxisome Proliferator-Activated Receptor (PPAR) Subtypes by Biochl. Bioph Res Comm. 2000; 278 (3):704-711.ISSN 0006-291X, https://doi.org/10.1006/bbrc.2000.3868.
- Singh G, Can AS & Correa R 2023 July 4; Copyright © 2025, StatPearls Publishing
- DeFronzo Banting Lecture. From the triumvirate to the ominous octet: a new paradigm for the treatment of type 2 diabetes mellitus. Diabetes 2009;58:773–795
- Gastaldelli A, Ferrannini E, Miyazaki Y, Matsuda M, Mari A, DeFronzo Thiazolidinediones improve beta- cell function in type 2 diabetic patients. Am J Physiol Endocrinol Metab 2007;292: E871–E883
- Giacaglia L, Barcellos C, Genestreti P, Silva M, Santos R, Vencio S, Bertoluci Tratamento farmacológico do prediabetes. Diretriz da Sociedade Brasileira de Diabetes 2023
- Dos Santos ESM, Máximo RO, de Andrade FB, de Oliveira C, Lima-Costa MF, Alexandre Differences in the prevalence of prediabetes, undiagnosed diabetes and diagnosed diabetes and associated factors in cohorts of Brazilian and English older adults. Public Health Nutr. 2021;24(13):4187-4194. doi:10.1017/S1368980020003201
- Cai X, Zhang Y, Li M, Wu J H, Mai L, Li J et Association between prediabetes and risk of all cause mortality and cardiovascular disease: updated meta-analysis BMJ 2020; 370 :m2297 doi:10.1136/bmj.m2297IDF 11th edition- Global diabetes report. https://www.diabetesatlas.org
- Gwira JA, Fryar CD & Quiuping Prevalence of Total, Diagnosed, and Undiagnosed Diabetes in Adults: United States, August 2021–August 2023. NCHS data Brief 516 Nov 2024
- Gast KB, Tjeerdema N, Stijnen T, Smit JW, Dekkers OM. Insulin resistance and risk of incident cardiovascular events in adults without diabetes: meta-analysis. PLoS One. 2012;7(12):e52036. doi: 1371/journal.pone.0052036.
- Zhang X, Li J, Zheng S, Luo Q, Zhou C, Wang Fasting insulin, insulin resistance, and risk of cardiovascular or all-cause mortality in non-diabetic adults: a meta-analysis. Biosci Rep. 2017 Sep 7;37(5):BSR20170947. doi: 10.1042/BSR20170947. PMID: 28811358; PMCID: PMC6448479.
- Brannick B, Dagogo-Jack S. Prediabetes and Cardiovascular Disease: Pathophysiology and Interventions for Prevention and Risk Reduction. Endocrinol Metab Clin North Am. 2018 Mar;47(1):33-50. doi: 10.1016/j.ecl.2017.10.001. PMID: 29407055; PMCID: PMC5806140.
- Mottillo S, Filion KB, Genest J, Joseph L, Pilote L, Poirier P, Rinfret S, Schiffrin EL, Eisenberg The metabolic syndrome and cardiovascular risk a systematic review and meta-analysis. J Am Coll Cardiol. 2010 Sep 28;56(14):1113-32. doi: 10.1016/j.jacc.2010.05.034. PMID: 20863953
- de Siqueira Valadares LT, de Souza LSB, Salgado Júnior VA, de Freitas Bonomo L, de Macedo LR, Silva M. Prevalence of metabolic syndrome in Brazilian adults in the last 10 years: a systematic review and meta- analysis. BMC Public Health. 2022 Feb 16;22(1):327. doi: 10.1186/s12889-022-12753-5. PMID: 35172790; PMCID: PMC8848905.
- Marx N, Rydén L, Federici M, Marx-Schütt K, Verket M, Müller-Wieland D et al. Great debate: pre-diabetes is not an evidence-based treatment target for cardiovascular risk reduction. Eur Heart J. 2024 Dec 23;45(48):5117- doi: 10.1093/eurheartj/ehae533. PMID: 39387537.
- Bergman M, Manco M, Satman I, Chan J, Schmidt MI, Sesti G, et International Diabetes Federation Position Statement on the 1-hour post-load plasma glucose for the diagnosis of intermediate hyperglycaemia and type 2 diabetes. Diabetes Res Clin Pract. 2024 Mar;209:111589. doi: 10.1016/j.diabres.2024.111589.
- Rinella ME, Lazarus JV, Ratziu V, Francque SM, Sanyal AJ, Kanwal F, et A multi-society Delphi consensus statement on new fatty liver disease nomenclature. J Hepatol. 2024;80(3):659-74.
- Lonardo A, Nascimbeni F, Mantovani A, Targher Hypertension, diabetes, atherosclerosis and NASH: Cause or consequence? J Hepatol. 2018. ;68(2):335-352.
- Rinella , Neuschwander-Tetri BA., Siddiqui MS., et al. AASLD Practice Guidance on the clinical assessment and management of nonalcoholic fatty liver disease. Hepatology 2023;77(5):1797–835.
- Younossi ZM, Zelber-Sagi S, Lazarus JV, Wong VW, Yilmaz Y, Duseja A, et al. Global Consensus Recommendations for Metabolic Dysfunction-Associated Steatotic Liver Disease and Steatohepatitis. 2025 ;169(5):1017-1032.e2).
- Cotrim HP, Parise ER, Figueiredo-Mendes C, Galizzi-Filho J, Porta G, Mello ES, et al. Nonalcoholic fatty liver disease in Brazil: Clinical and histological profile. Ann Hepatol. 2011;10(1):33-9.
- Rocha S, Oliveira CP, Stefano JT, Yokogawa RP, Gomes-Gouvea M, Zitelli PMY, et.al. Polymorphism's MBOAT7 as Risk and MTARC1 as Protection for Liver Fibrosis in Int J Mol Sci. 2025 3;26(13):6406.
- Fu S, Groothuismink ZMA, Balderramo D, Mattos AZ, Hoppe L, Carrera E, et al. Genetic risk score correlates with immune profile and risk of HCC and cirrhosis development in Hispanics with MASLD. HEP Rep. 2025 2;7(10):101508
- Younossi ZM, Paik JM, Lazarus JV, Burra P, Eguchi Y, Tacke F et Projected Global Clinical, Humanistic, and Economic Impact of Metabolic Dysfunction-Associated Steatohepatitis (MASH): The Cost of Inaction Based on Data From Nine Countries. Clin Gastroenterol Hepatol 2025 (in press).
- Diaz LA, Arab JP, Idalsoaga F, Perelli J, Veja J, Dirchwolf M et al. Updated recommendations for the management of metabolic dysfunction-associated steatotic liver disease (MASLD) by the Latin American working group. Ann Hepatol. 2025 Jul-Dec;30(2):101903. doi: 10.1016/j.aohep.2025.101903.
- Ahmad E, Lim S, Lamptey R, Webb DR, Davies MJ. Type 2 diabetes. Lancet. 2022;400(10365):1803-1820. doi:10.1016/S0140-6736(22)01655-5.
- Godoy-Matos AF, Valério CM, Júnior WSS, de Araujo-Neto JM, Sposito AC, Suassuna JHR. CARDIAL-MS (CArdio-Renal-DIAbetes-Liver-Metabolic Syndrome): a new proposition for an integrated multisystem metabolic disease. Diabetol Metab Syndr. 2025;17(1):218. Published 2025 Jun 16. doi:10.1186/s13098-025-01796-4
- Ahlqvist E, Storm P, Käräjämäki A, Martinell M, Dorkhan M, Carlsson A, et Novel subgroups of adult-onset diabetes and their association with outcomes: a data-driven cluster analysis of six variables. Lancet Diabetes Endocrinol. 2018 May;6(5):361-369. doi: 10.1016/S2213-8587(18)30051-2.
- Udler MS, Kim J, von Grotthuss M, Bonàs-Guarch S, Cole JB, Chiou J et al. Type 2 diabetes genetic loci informed by multi-trait associations point to disease mechanisms and subtypes: A soft clustering PLoS Med. 2018 Sep 21;15(9):e1002654. doi: 10.1371/journal.pmed.1002654. PMID: 30240442.
- Ortega HI, Udler MS, Gloyn AL, Sharp Diabetes mellitus polygenic risk scores: heterogeneity and clinical translation. Nat Rev Endocrinol. 2025 Sep;21(9):530-545. doi: 10.1038/s41574-025-01132-w. PMID: 40467969; PMCID:.
- Knop A gut feeling about glucagon. Eur J Endocrinol. 2018 Jun;178(6):R267-R280. doi: 10.1530/EJE-18- 0197.
- Richter MM, Galsgaard KD, Elmelund E, Knop FK, Suppli MP, Holst JJ, et The Liver-α-Cell Axis in Health and in Disease. Diabetes. 2022 Sep 1;71(9):1852-1861. doi: 10.2337/dbi22-0004. PMID: 35657688; PMCID: PMC9862287.
- Taylor Pathogenesis of type 2 diabetes: tracing the reverse route from cure to cause. Diabetologia. 2008;51:1781–1789. doi: 10.1007/s00125-008-1116-7.
- Alam F, Islam MA, Mohamed M, Ahmad I, Kamal MA, Donnelly R, Idris I, Gan SH. Efficacy and Safety of Pioglitazone Monotherapy in Type 2 Diabetes Mellitus: A Systematic Review and Meta-Analysis of Randomised Controlled Sci Rep. 2019 Mar 29;9(1):5389. doi: 10.1038/s41598-019-41854-2. PMID: 30926892; PMCID: PMC6441028
- Sanyal AJ, Chalasani N, Kowdley KV, McCullough A, Diehl AM, Bass MN et Pioglitazone, Vitamin E, or Placebo for Nonalcoholic Steatohepatitis. N Engl J Med 2010 May 6;362(18):1675-1685 DOI: 10.1056/NEJMoa0907929
- Pereira IVA, de Oliveira ABS, Zitelli PMY, Barbieri LA, Cardoso AC, Monteiro MJSD et . Long-term pioglitazone uses in MASLD patients: insights from a multicentric preliminary study. Clinics 2025 21;80: 100737.
- Musso G, Cassader M, Paschetta E, Gambino Thiazolidinediones and Advanced Liver Fibrosis in Nonalcoholic Steatohepatitis: A Meta-analysis. JAMA Intern Med. 2017;177(5):633-40
- Panunzi S, Maltese S, Verrastro O, Labbate L, De Gaetano A, Pompili M, et al. Pioglitazone and bariatric surgery are the most effective treatments for non-alcoholic steatohepatitis: A hierarchical network meta-analysis. Diabetes Obes Metab. 2021;23(4):980-90.
- American Diabetes Association Professional Practice Committee for Diabetes* . Prevention or Delay of Diabetes and Associated Comorbidities: Standards of Care in Diabetes-2026. Diabetes Care. 2026;49(Supplement_1):S50-S60. doi:10.2337/dc26-S003
- Ipsen EØ, Madsen KS, Chi Y, et al. Pioglitazone for prevention or delay of type 2 diabetes mellitus and its associated complications in people at risk for the development of type 2 diabetes Cochrane Database Syst Rev. 2020;11(11):CD013516. Published 2020 Nov 19. doi:10.1002/14651858.CD013516.pub2
- Ostrominski JW, Højbjerg Lassen MC, Claggett BL, et Sodium-glucose co-transporter 2 inhibitors and new- onset diabetes in cardiovascular or kidney disease. Eur Heart J. 2025;46(14):1321-1331. doi:10.1093/eurheartj/ehae780
- Li L, Lui DT, Fong CH, et Benefits of glucagon-like peptide-1 receptor agonists versus pioglitazone for cardio- hepatic outcomes: a territory-wide target trial emulation. Cardiovasc Diabetol. 2025;24(1):416. Published 2025 Oct 31. doi:10.1186/s12933-025-02973-5
- Kernan WN, Viscoli CM, Furie KL, et Pioglitazone after Ischemic Stroke or Transient Ischemic Attack. N Engl J Med. 2016;374(14):1321-1331. doi:10.1056/NEJMoa1506930
- Zhou Y, Huang Y, Ji X, Wang X, Shen L, Wang Pioglitazone for the Primary and Secondary Prevention of Cardiovascular and Renal Outcomes in Patients with or at High Risk of Type 2 Diabetes Mellitus: A Meta- Analysis. J Clin Endocrinol Metab. 2020;105(5):dgz252. doi:10.1210/clinem/dgz252
- Dormandy JA, Charbonnel B, Eckland DJ, Erdmann E, Massi-Benedetti M, Moules IK et al. Secondary prevention of macrovascular events in patients with type 2 diabetes in the PROactive Study (PROspective pioglitAzone Clinical Trial In macroVascular Events): a randomised controlled trial. 2005 Oct 8;366(9493):1279-89. doi: 10.1016/S0140-6736(05)67528-9. PMID: 16214598.
- Baddam S, Banka AV, Divity S, Sandesara M, Vityala Association between pioglitazone use and bladder cancer: A systematic review. Bladder. 2024;11(4):e21200023. DOI: 10.14440/bladder.2024.0039
- Erdmann, , Song, E., Spanheimer, R., van Troostenburg de Bruyn, AR, Perez, A. Observational follow-up of the PROactive study: a 6-year update. Diabetes Obes Metab,2014; 16: 63-
- https://doi.org/10.1111/dom.12180
- Erdmann E, Harding S, Lam H, Perez Ten-year observational follow-up of PROactive: a randomized cardiovascular outcomes trial evaluating pioglitazone in type 2 diabetes. Diabetes Obes Metab. 2016 Mar;18(3):266-73. doi: 10.1111/dom.12608. Epub 2016 Jan 8. Erratum in: Diabetes Obes Metab. 2017 Jun;19(6):912. doi: 10.1111/dom.12965. PMID: 26592506.
- Lewis JD, Habel LA, Quesenberry CP, Strom BL, Peng T, Hedderson MM et Pioglitazone Use and Risk of Bladder Cancer and Other Common Cancers in Persons With Diabetes. JAMA. 2015 Jul 21;314(3):265-77. doi: 10.1001/jama.2015.7996. PMID: 26197187.
- Marx N, Federici M, Schütt K, et 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023;44(39):4043-4140. doi:10.1093/eurheartj/ehad192
- UNITED Food and Drug Administration. Pioglitazone and metformin hydrochloride: FDA drug label. Atualizado em: 16 set. 2025.
- Clarke GD, Solis-Herrera C, Molina-Wilkins M, Martinez S, Merovci A, Cersosimo E, et al. Pioglitazone Improves Left Ventricular Diastolic Function in Subjects With Diabetes Care. 2017 Nov;40(11):1530- 1536. doi: 10.2337/dc17-0078.
- Moody AJ, Molina-Wilkins M, Clarke GD, Merovci A, Solis-Herrera C, Cersosimo E, et al. Pioglitazone reduces epicardial fat and improves diastolic function in patients with type 2 Diabetes Obes Metab. 2023 Feb;25(2):426-434. doi: 10.1111/dom.14885. Epub 2022 Nov 4. PMID: 36204991; PMCID: PMC9812869.
- Forner P, Sheu Bone Health in Patients With Type 2 Diabetes. J Endocr Soc. 2024;8(7):bvae112. Published 2024 Jun 6. doi:10.1210/jendso/bvae112
- Fernández-Pombo A, Ossandon-Otero JA, Guillín-Amarelle C, et Bone mineral density in familial partial lipodystrophy. Clin Endocrinol (Oxf). 2018;88(1):44-50. doi:10.1111/cen.13504
- American Diabetes Association Professional Practice Committee for Diabetes*; 4. Comprehensive Medical Evaluation and Assessment of Comorbidities: Standards of Care in Diabetes—2026. Diabetes Care 1 January 2026; 49 (Supplement_1): S61–S88. https://doi.org/10.2337/dc26-S004
- Colhoun HM, Livingstone SJ, Looker HC, et al. Hospitalised hip fracture risk with rosiglitazone and pioglitazone use compared with other glucose-lowering Diabetologia. 2012;55(11):2929-2937. doi:10.1007/s00125-012-2668-0
- Shadid S, Jensen Effects of Pioglitazone Versus Diet and Exercise on Metabolic Health and Fat Distribution in Upper Body Obesity. Diabetes Care 1 November 2003; 26 (11): 3148–
- https://doi.org/10.2337/diacare.26.11.3148
- White U, Fitch MD, Beyl RA, Hellerstein MK, Ravussin E. Adipose depot-specific effects of 16 weeks of pioglitazone on in vivo adipogenesis in women with obesity: a randomised controlled Diabetologia. 2021 Jan;64(1):159-167. doi: 10.1007/s00125-020-05281-7. Epub 2020 Oct 1. PMID: 33001232; PMCID: PMC7718382.
Inzucchi, S.E., Viscoli, C.M., Young, L.H. et al. Diabetes prevention and cardiovascular



